Pero vamos allá con lo que normalmente no nos suelen contar en la escuela sobre los electrones.
Él no lo sabía pero, debido al frotamiento, algunos electrones de la lana se habían quedado en la superficie del ámbar y lo habían dotado de un exceso de carga eléctrica negativa que, cuando se acercaba a la pluma (que es neutra porque tiene dentro igual número de cargas + y -), era capaz de atraer hacia sí sus cargas positivas haciendo que se quedase pegada: ¡algo desconocido había "anulado" el peso del objeto y a ese algo le llamaron electricidad!
2ª. El descubrimiento del electrón destrozó el significado etimológico de la palabra átomo pero... ¡le abrió a la humanidad las puertas para conocer en profundidad la estructura interna de la materia!
La palabra átomo proviene de dos vocablos griegos: "a", que significa 'sin", y "tomon", "división". Luego un átomo, literalmente, sería algo sin posibilidad de poder ser dividido en partes más pequeñas. Esto requeriría carecer de partes en su interior. Pues bien, como veremos, la forma en que se descubrió el electrón implica que este se encuentra en el átomo y se acaba separando de él. Por tanto, el átomo no es una partícula indivisible como su nombre original quería indicarnos.
Aún así, la denominación átomo se ha mantenido por su fuerte arraigo y porque sigue siendo la partícula más pequeña que es capaz de mostrar todas las propiedades fijas atribuibles a un determinado elemento químico (masa, volumen, comportamiento químico, etc.)
Esta
ilustración adaptada por los compañeros de la muy recomendable
web https://fisiquimicamente.com/ nos ayudará a comprender por qué se puede concluir que hay una partícula de carga negativa que cuando es forzada a abandonar el átomo nos demuestra que el átomo tiene partes en su interior y es por ello divisible en otras partículas menores. Dicha partícula es el
electrón y el
experimento con el que se descubrió lo diseñó el científico británico
J.J. Thomson.
La intensa fuerza eléctrica producida por el generador (una potente pila) arranca electrones de los átomos del cátodo (metal conectado al polo - de la pila) y los envía en línea recta formando un rayo hacia el ánodo (otro metal distinto del primero y que se conecta al polo +).
A estos rayos formados por un flujo de electrones, como parten desde el cátodo, se les conoce como rayos catódicos y, como en el tubo se ha hecho el vacío, sus electrones no pueden provenir más que de haberse desgajado de los átomos que constituyen el cátodo. Thomson dedujo que su carga era negativa porque eran atraídos por el polo + de la pila, pero se cercioró de ello añadiendo otra pila más y observando como se desviaban hacia el polo +:
Pero el punto clave es este: repitió el experimento con cátodos y ánodos hechos de otros elementos químicos, y resultó que la partícula que formaba los rayos catódicos era siempre la misma ya que tenía siempre el mismo tipo de desviación hacia el polo + y la misma relación de carga/masa). Ello indicaba que dicha partícula de carga eléctrica negativa era un constituyente fundamental de la materia. Es decir, que... ¡el electrón estaba presente en todos y cada uno de los átomos del universo!
Thomson, en principio, lo llamó corpúsculo pero, al estar claro que lo sucedido en su experimento era un fenómeno eléctrico, se acabó imponiendo el término electrón, el cual ya había sido propuesto varios años antes por el físico irlandés Stoney como hipótesis para designar al hipotético corpúsculo que transportarba la electricidad de unos materiales a otros.
Finalmente, como la mayoría de la materia con la que tratamos cotidianamente no nos da calambre, debemos concluir que es eléctricamente neutra, por lo que dentro de los átomos debía haber necesariamente al menos otro tipo de partícula de carga positiva que contrarrestase la negativa del electrón. Y los científicos de la época se lanzaron como locos a descubrirla hasta que Rutherford en 1911 consiguió detectar el protón bombardeando una fina lámina de oro con partículas alfa. Poco más tarde, en 1932 Chadwick descubriría la tercera partícula fundamental del átomo, el neutrón.
Todo este conocimiento sobre la estructura del átomo resultaría trascendental a lo largo del siglo XX para poder manipular internamente la materia y lograr con ello un desarrollo científico y tecnológico espectacular en beneficio de la humanidad.
3ª Al electrón lo descubrió Thomson en 1897 pero... en realidad fue "un caso temprano de ciencia colectiva" y... ¡ni siquiera era lo que él andaba buscando! (Jaume Navarro, historiador de la ciencia).
Parafraseando a Newton con sus Leyes del Movimiento, Thomson también se apoyó en hombros de gigantes para descubrir al electrón. Veamos qué otros científicos aportaron el conocimiento necesario para su hallazgo:
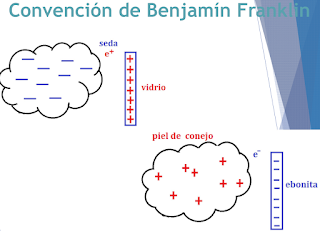
- Siglo XVIII: Los experimentos de Benjamin Franklin frotando el vidrio contra la seda y la ebonita (plástico procedente del caucho) contra la piel de conejo demostraron que la materia se podía cargar eléctricamente de dos maneras distintas a las que propuso llamar carga positiva y carga negativa.
Cuando Franklin acercaba una varilla de vidrio a la ebonita ambas se atraían. Cuando acercaba dos varillas iguales ambas se repelían. Concluyó que tanto el vidrio frotado como la ebonita frotada presentan electricidad pero son de naturalezas diferentes. Arbitrariamente llamó positiva a la del vidrio frotado y negativa a la de la ebonita frotada.
- Mediados del siglo XIX: Laming es el primero en hipotetizar que en el átomo hay partículas con una carga eléctrica unitaria rodeando a un núcleo material y que dicho átomo se carga al añadirlas o eliminarlas.
- Finales del siglo XIX: en la comunidad científica saltan chispas. Faraday ha descubierto con la electrólisis que pasándole electricidad a ciertas ciertas sales en disolución puede obtener libres los elementos que las componen e introduce los términos ión, catión y anión para designar las especies cargadas que gracias a la electricidad se mueven en disolución hacia el cátodo y el ánodo.
Electrólisis: los iones de una sustancia disuelta se depositan unos sobre el cátodo y otros sobre el ánodo, que son dos varillas metálicas conectadas a una pila que se introducen en la disolución. En el proceso hay reacciones químicas que implican transferencias de electrones entre las especies químicas participantes
Stoney propone llamar electrón a esa hipotética carga eléctrica unitaria de la que habló Laming.
Goldstein descubre los rayos catódicos que viajan en unos tubos de vacío que había diseñado
Crookes y, este último,
había probado que su naturaleza era de carga negativa porque se desviaban hacia el polo + tras aplicarles perpendicularmente un campo eléctrico.
Todo esto nos suena del experimento de Thomson que hemos descrito antes, ¿verdad? Pues nada, su investigación principal, y por la que recibió el premio Nobel de Física en 1906, fue la conducción de la electricidad a través de tubos llenos con distintos gases.
Así, ahondando en los mecanismos de interacción entre la materia y aplicando la Teoría Electromagnética de Maxwell, se puso a buscar el valor mínimo de carga en la electricidad cuando se percató de algo mucho más trascendental: independientemente del material del que estuviese hecho el cátodo, siempre salía desde él la misma partícula con la misma cantidad de carga negativa y con la misma masa, o sea, era una partícula potencialmente presente en todos los átomos: el electrón.
Esto fue sorprendente no solo para él y para todo el mundo porque el átomo se creía indivisible y no podía descartarse que el electrón fuese simplemente una partícula portadora de la electricidad independiente de los átomos que viajaba entre ellos transportando la electricidad.
4ª El electrón no está formado por la combinación de otras partículas menores dentro de él, como sí les ocurre al protón y el neutrón...¡él sí que es un tío de una sola pieza!
Protón = 2 quarks arriba + 1 quark abajo Neutrón = 2 quarks abajo + 1 quark arriba u viene de up, arriba en inglés d viene de down, abajo en inglés
Como podemos ver en la figura, el electrón no tiene componentes internos, mientras que los protones y neutrones sí que los tienen: están formados por combinaciones de quarks, unas partículas aún más diminutas que propuso el Modelo Estándar de partículas, hasta ahora el más fiable para explicar cuáles son los constituyentes últimos de la materia y de la energía. Y lo hace postulando tres tipos de partículas fundamentales e indivisibles: quarks, leptones y bosones.
- Los quarks son partículas que van siempre en grupo, unidos entre sí gracias a la fuerza nuclear para formar partículas subatómicas más grandes llamadas hadrones, dos de las cuales son el protón y el neutrón. Hay 6 tipos o sabores de quarks (sí, no se venden en el súper pero ya sabemos que los físicos suelen ser unos señores más bien raretes) y tienen nombres un tanto exóticos: arriba, abajo, encanto, extraño, superior e inferior.
- Los leptones son partículas solitarias que no se combinan entre sí. A este grupo pertenece el electrón, que es además la más ligera de todas las partículas elementales.
Quarks y leptones son los constituyentes de la materia existente en el universo.
- Y finalmente están los bosones, unas partículas que cuando son virtuales (o sea, que existen durante un tiempo tan corto que es imposible observarlas) son muy importantes porque hacen que la materia pueda experimentar los distintos tipos de fuerza que conocemos. Digamos que cuando un par de quarks o leptones se intercambian un bosón virtual este les transmite una fuerza que ellos acaban experimentando. Los bosones virtuales son pues los portadores o transmisores de las fuerzas que sufre la materia.
Existen 4 tipos de fuerzas fundamentales en el universo: gravitatoria, electromagnética, nuclear débil y nuclear fuerte. Pues bien, en cada una de ellas, los quarks y los leptones intercambian un bosón determinado y como resultado de ello sufren el tipo de fuerza correspondiente. Precisar que el bosón llamado gravitón aún no se ha detectado en la realidad.
Las 4 fuerzas según el Modelo Estándar
Por ejemplo, cuando dos electrones se acercan y se repelen, el Modelo Estándar lo explica porque uno de ellos altera el campo electromagnético en el que se encuentra y emite un fotón virtual que acaba chocando con el otro electrón y desapareciendo. Como resultado de este intercambio energético ambos electrones modifican las direcciones de sus respectivos movimientos y se separan el uno del otro.
También existen bosones, como por ejemplo los fotones que forman la luz visible o cualquier otra clase de radiación electromagnética que son partículas reales que sí existen durante largo tiempo e interactúan con la materia de diversos modos: calentándola, provocándole electricidad (efecto fotoeléctrico), etc.
En el siguiente esquema están todas las partículas elementales que forman el universo según el Modelo Estándar:
5ª Cerca del electrón pueden surgir y detectarse partículas de "la nada": ¡el vacío no está tan vacío!
Esto ocurre gracias a lo que se conoce como fluctuaciones cuánticas del vacío. Imaginemos una zona a escala nanométrica, o sea, más pequeña que un átomo, donde no haya nada de materia. Si le bajamos la temperatura casi al cero absoluto y conseguimos que no le llegue de fuera radiación electromagnética de ningún tipo, tendremos un vacío casi perfecto carente de materia y , aparentemente, también de energía.
En esas condiciones, se ha podido comprobar (experimento de Benea - Chelmus) que de esa aparente nada es capaz de surgir durante unos brevísimos instantes (10-21 segundos) una pequeña cantidad de energía que, siguiendo la famosa ecuación de Einstein que nos dice que energía y masa son, en el fondo, una misma realidad interconvertible la una en la otra ( E = m c2 ), es capaz de transformase en billones de pares de partículas electrón - positrón (un positrón tiene la misma masa que un electrón pero carga positiva) que chocan inmediatamente entres sí para transformarse otra vez en una energía que al siguiente instante ya no se detecta pero que poco después puede volver a aparecer y a repetir el fenómeno. A este baile perpetuo de aparición y extinción de energía en "la nada" es a lo que llamamos fluctuaciones cuánticas del vacío.
Pues bien, una manera simple de detectar dichas fluctuaciones es porque, durante el brevísimo instante que apuntamos antes, cerca de un electrón permanente (de los normales de la materia, de los que no aparecen y desaparecen como pares electrón - positrón) se produce una disminución del campo eléctrico que este creaba a su alrededor y que es perfectamente medible con la tecnología actual.
La razón por la que disminuye el campo eléctrico que nos permite saber que ha habido una fluctuación cuántica del vacío es muy fácil de entender: antes de que surgiera la fluctuación no había pares electrón-positrón y el campo eléctrico no encontraba obstáculos para transmitirse, pero cuando esta surge el campo eléctrico debe atravesar esa especie de pantalla que forma el espacio polarizado creado por los pares electrón-positrón, entonces le cuesta más transmitirse y su valor decrece.
Nota: decimos "espacio polarizado" porque, como se puede ver en la figura, debido a la atracción eléctrica, el par se sitúa con el positrón (+) en el polo más cercano al "electrón permanente" y el electrón en el opuesto. Es la llamada polarización cuántica.
En el siguiente enlace puedes conocer otras cinco curiosidades más sobre nuestro amigo el electrón 😃
"Sólo la cultura da libertad...sólo el que sabe es libre, y más libre el que más sabe"
D. Miguel de Unamuno
Esta es, en última instancia, la razón de ser de este modesto blog.
¡Gracias por leerlo y ayudar a su difusión!
BIBLIOGRAFÍA












.png)


Muy fácil de entender y la vez tan rico en información . ¡ UN TRABAJO CURIOSO Y ÚTIL¡ Muchas gracias
ResponderEliminarMuchas gracias, me alegro mucho de que le haya gustado.
Eliminar